Perkembangan Teori Atom Dalton sampai dengan Bohr
Perkembangan Teori Atom Dalton sampai dengan Bohr - Konsep atom sebagai partikel terkecil di alam semesta, dicetuskan oleh Demokritos di masa Yunani Kuno. Namun karena teori itu tak disertai penelitian ilmiah, banyak ilmuwan yang meragukan dan meneliti kebenarannya. Gagasan yang disampaikan oleh Democritus menyatakan bahwa bila suatu materi dibagi menjadi bagian yang paling kecil lagi lalu terus dibagi lagi dimana akan sampai suatu bagian yang sangat kecil yang tidak dapat dibagi lagi atau tidak dapat dihancurkan disebut atom (Dari kata Atomos dalam Bahasa Yunani yang artinya tak terbagi).
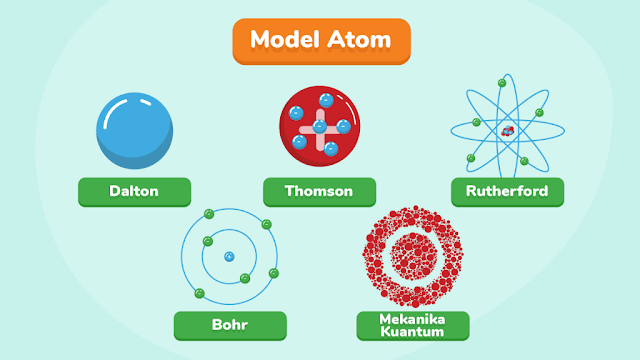
Baru pada abad ke-19, atom diteliti secara ilmiah. Perkembangan Teori Atom: Model Dalton, Thomson, Rutherford, dan Bohr
Teori atom Dalton
Perkembangan teori atom pertama dicetuskan oleh John Dalton pada tahun 1803 hingga 1808. John Daton menyatakan bahwa
- Setiap unsur terdiri dari partikel yang sangat kecil yang disebut atom
- Semua atom dari satu unsur yang sama adalah identik, namun atom unsur lain berbeda dengan unsur-unsur lainnya
- Atom tidak dapat dibagi, tidak dapat diciptakan ataupun dimusnakan melalui reaksi kimia.
- Senyawa terbentuk dari gabungan atom dari unsur-unsur berbeda dengan perbandingan rasio atom yang spesifik
Model atom Dalton digambarkan sebagai bola pejal atau model bola billiard seperti gambar berikut.

Teori Atom J.J. Thomson
Teori atom J.J. Thomson lahir pada tahun 1897 saat ia melakukan eksperimen dengan sinar katoda. Dalam eksperimennya, sinar katoda dapat terbelokan oleh suatu medan magnet ataupun medan listrik. Sinar katoda yang bermuatan listrik dapat dapat terbelokkan menuju kea rah kutub bermuatan positif sehingga sinar katoda bermuatan negatif.
Nah, partikel bermuatan negatif inilah mengacu pada penemuan electron dan J.J. Thomson berpendapat bahwa atom terdiri dari electron-elektron bermuatan negatif.

Model atom J.J. Thomson digambarkan dengan bola dengan elektron yang terseber seperti roti kismis. Kismis-kismis ini adalah electron-elektron sedangkan rotinya adalah bola bermuatan positif..
Teori Atom Rutherford
Pada tahun 1911, Ernest Rutherford melakukan eksperimen dengan menembakkan partikel α partikel bermuatan positif pada lempeng emas tipis.
Dari eksperimen tersebut, dia menemukan bahwa sebagian besar partikel menembus melewati lempengan emas, kemudian sebagian lainnya mengalami pembelokan dan terpantulkan.

Disimpulkan bahwa model Atom Rutherford terdiri dari atom yang sebagian besar merupakan ruang kosong yang berbentuk inti padat dan bermuatan positif disebut inti atom dan elektron-elektron bermuatan negatif yang mengitari inti atom.
Teori Atom Bohr
Pada tahun 1913, Niels Bohr mengajukan gagasan model atom untuk menjelaskan fenomena Hamburan sinar dari unsur-unsur ketika dikenakan pada nyala api ataupun tegangan listrik tinggi.
Model atom Bohr secara khusus merupakan model atom hidrogen untuk menjelaskan fenomena spektrum garis atom hidrogen. Bohr menyatakan bahwa elektron-elektron bermuatan negatif bergerak mengelilingi inti atom bermuatan positif pada jarak tertentu yang berbeda-beda seperti halnya orbit planet mengelilingi matahari.

Nah, model atom Bohr juga dikenal sebagai model tata surya. Dalam model ini setiap lintasan orbit elektron berada tingkat energi yang berbeda dimana semakin jauh lintasan orbit dari inti, semakin tinggi tingkat energi. Lintasan orbit elektron ini disebut kulit elektron. Saat elektron jatuh dari orbit yang lebih luar ke orbit yang lebih dalam, sinar yang diradiasikan bergantung pada tingkat energi dari kedua lintasan orbit tersebut.
Teori Mekanika Kuantum
Teori Mekanika Kuantum diawali dengan “bencana ultraviolet” menjelang akhir abad ke 19. Pada frekuensi tinggi, radiasi benda hitam akan bernilai sangat besar bahkan tak terhingga. Max Planck berhasil menemukan rumusan sederhana tentang radiasi benda hitam untuk mengatasi masalah bencana ultraviolet ini.
Walaupun sederhana, penemuan inilah yang mendasari lahirnya fisika kuantum di awal abad 20.
Pada waktu yang bersamaan, Albert Einstein mengirimkan makalah kepada Planck yang berisi gagasan efek fotolistrik pada tahun 1905. Gagasan Einstein ini membuktikan rumusan sederhana Planck dan membuktikan bahwa cahaya berperilaku sebagai partikel. Setelah itu, ada Fisikawan asal Amerika Serikat bernama Arthur Compton yang turut ikut andil dalam membuktikan bahwa cahaya mempunyai dua perilaku yaitu partikel dan gelombang.
Seiring dengan waktu, Louis de Broglie berhasil merumuskan momentum linier sebuah gelombang. Hal ini yang menjadikan sebuah gelombang dapat berperilaku juga sebagai partikel.










Post a Comment